2023年8月8日,中國科學院上海藥物研究所張繼穩團隊與臨港實驗室殷憲振研究員、江西中醫藥大學Abid Naeem博士等合作,受邀在ACS Molecular Pharmaceutics上發表了題為“Advances in Structure Pharmaceutics from Discovery to Evaluation and Design”的綜述當期封面文章。
隨著對制劑結構的深入研究及經驗積累,結構藥劑學的研究重點由制劑結構的發現,逐步轉向探究制劑結構對藥物的釋放、靶向特征的影響及其與生物體內復雜結構的相互作用,“知其所見”,通過藥物遞送系統的內部結構、定量結構,加深對結構化的釋藥機制的理解。例如,通過觀測滲透泵片釋放過程中結構演變,提出了雙層滲透泵片藥物釋放新模型——“地下河”藥物釋放模型,提出了符合滲透泵片由結構決定的釋藥機制(圖2 A)。利用同步輻射光源顯微斷層掃描成像,凝膠骨架片釋放過程中結構的演變清晰可見,整體呈現出溶蝕層、擴散層和溶脹層的典型結構(圖2 B)。此外,生物體內復雜的組織生理結構、病理結構也影響著藥物遞送系統的體內命運。例如,由于呼吸系統氣管樹結構復雜,經口吸入藥物微粒在肺內的沉積也受其影響,研究表明干粉吸入微粒在小鼠肺內的沉積呈現出顯著的分布差異,右肺下葉藥物沉積量多于其他肺葉(圖2 C)。
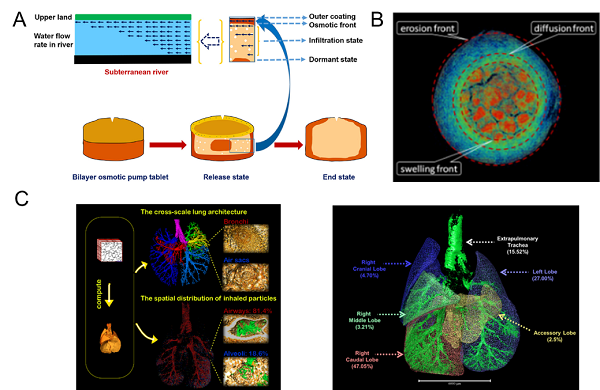
圖2 藥物遞送系統結構及微粒制劑在體內的空間分布特征:
(A)滲透泵片“地下河”藥物釋放模型;(B)凝膠骨架片藥物釋放結構演變;(C)呼吸道結構對吸入微粒在肺內沉積的作用
利用前期研究成果與經驗,現階段結構藥劑學研究正著力于制劑的評價與開發,設計新劑型,構建以制劑結構為基礎的藥品監管方法,“知以致用”。評估制劑的體內外相關性是一項重要的任務,體外溶出試驗是最常用的評價制劑釋放行為的方法,但很少關注制劑在體內溶出時的結構變化。研究者嘗試從制劑結構出發,提出基于制劑結構的體內外相關性評價,并依據此策略,研究結構在動物體內的結構特征與其在體外釋放度測定介質中的結構特征及其相關性,為體內外相關性評價提供新策略(圖3 A-B)。基于制劑結構的評價策略也可以用于檢測片劑中的裂縫,相比于其他評價方法在此類檢測中具有無可替代的優越性(圖3 C)。
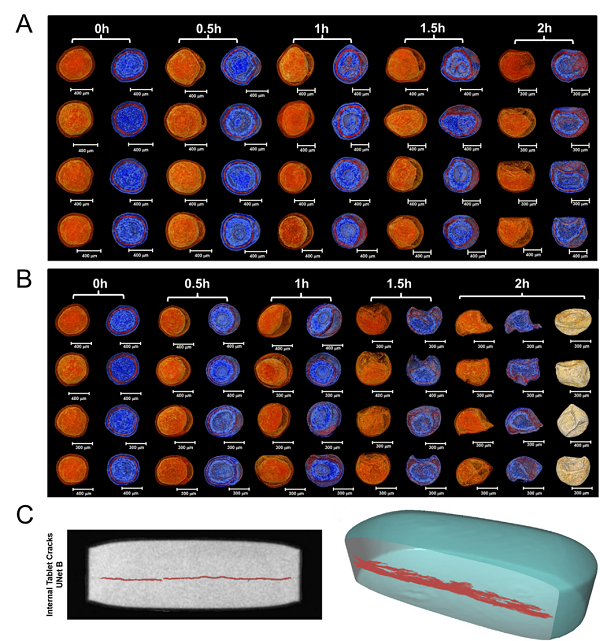
圖3 以結構為基礎的制劑評價:(A)腸溶微丸在體外溶出過程的結構演變;(B)腸溶微丸在體內溶出過程的結構演變;(C)片劑中縫隙的檢測
主要貢獻者與致謝
中國科學院上海藥物研究所碩士研究生許慧鵬、伍麗副研究員和中國科學院上海高等研究院薛艷玲研究員為本文共同第一作者。本文由中國科學院上海藥物所張繼穩研究員、臨港實驗室殷憲振研究員和江西中醫藥大學Abid Naeem博士共同指導。
全文鏈接:https://pubs.acs.org/doi/10.1021/acs.molpharmaceut.3c00514




 17312606166
17312606166