在一項新的研究中,來自美國范安德研究所、瑞典隆德大學和意大利佛羅倫薩大學的研究人員開發一種將使人們能夠更好地了解阿爾茨海默病如何在大腦中進展的新模型。相關研究結果近期發表在Acta Neuropathologica Communications期刊上,論文標題為“Proteomic analysis across patient iPSC-based models and human post-mortem hippocampal tissue reveals early cellular dysfunction and progression of Alzheimer’s disease pathogenesis”。

與其他神經退行性疾病一樣,阿爾茨海默病的研究也極具挑戰性。它極其復雜,發病時間長,而且因人而異。至關重要的是,科學家們還缺乏監測人類大腦中疾病進展的非侵入性技術。相反,他們往往依賴于模擬這種疾病的模型來跟蹤阿爾茨海病的產生及其影響大腦的方式。
論文共同通訊作者、范安德研究所副教授Laurent Roybon 博士說,“模型要發揮作用,就必須密切反映阿爾茨海默病在現實生活中的進展方式。我們的新模型再現了這一過程的許多關鍵方面。這項新研究的優勢之一是我們使用了源自阿爾茨海默病患者的細胞系,這有助于我們在這種模型中更好地反映實際的疾病過程。”
這種新模型利用了誘導性多能干細胞(induced pluripotent stem cell, iPSC)。在此基礎上,人們可以誘導iPSC細胞變成神經元等其他類型的細胞。這種強大的技術讓科學家們可以研究與患者具有相同遺傳背景的人類腦細胞。
然而,在大腦微環境之外研究這些細胞又是一個挑戰。腦細胞得益于一個受到嚴格調節的能促進細胞健康和功能的生態系統。為了解決這個問題,這些作者使用源自阿爾茨海默病患者的 iPSC來產生腦細胞。他們然后將這些腦細胞移植到免疫缺陷的野生型小鼠的大腦中,并監測阿爾茨海默病特征性病變---蛋白斑塊和纏結物、炎癥、線粒體功能障礙以及病變在整個大腦中移動的能力---的發展情況。
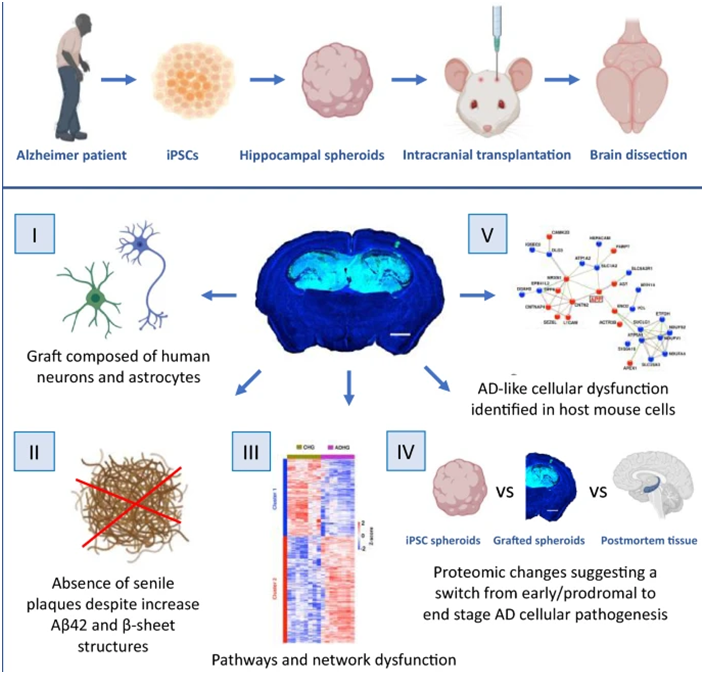
圖片來自Acta Neuropathologica Communications, 2023, doi:10.1186/s40478-023-01649-z。
這些作者發現,該模型成功再現了大腦通路中可能會導致淀粉樣蛋白斑塊形成的關鍵變化,還再現了鄰近腦細胞中與疾病相關的變化,這是疾病病理可能在細胞間擴散的跡象。蛋白質組分析還揭示了從疾病早期到晚期的變化。
這種新模型解決了阿爾茨海默病研究中的一個核心問題:盡管體外細胞模型和小鼠模型長期以來一直在幫助研究這種疾病,但將兩者結合起來能更準確地反映這種疾病在人類身上的產生和進程。這類模型被稱為嵌合模型,結合了體外細胞模型和小鼠模型的優勢。
Roybon說,下一步將監測細胞病理學如何在更長的時間范圍內發展,并研究病理學如何根據導致阿爾茨海默病的多種基因突變而有所不同。此外,這些作者還計劃解決他們的新模型的局限性,比如產生更能反映大腦特定區域細胞群體的 iPSC細胞。




 17312606166
17312606166