全球高達4億多人飽受糖尿病困擾,其中我國糖尿病患病人數居全球之首,已超1.3 億,占全國總人口的 9.4%[1]。胰高血糖素樣肽-1受體(glucagon-like peptide-1 receptor, GLP-1R)是治療2型糖尿病最有效的靶點之一。
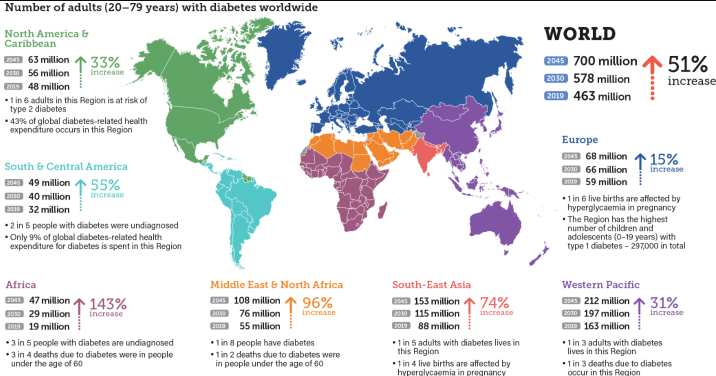
圖1 全球糖尿病患者統計
昨日(8月18日)信達生物的新型GLP-1R/GCGR雙激動劑IBI362 (LY3305677)一期臨床結果在國際知名期刊柳葉刀子刊EClinicalMedicine上發表。今年4月,諾和諾德的GLP-1R激動劑多肽司美格魯肽注射液在國內上市,每周只需皮下注射1次。目前國內上市的GLP-1R激動劑類藥物達到8款,它們不僅降糖效果顯著,同時還兼具減重、降壓、改善血脂譜等作用。近年來GLP-1R激動劑類藥物市場規模不斷增長,2020年全球市場規模已達100億美元。
GLP-1R為何能在2型糖尿病治療上大放異彩,今天小編帶大家一探究竟。
GLP-1R簡介
GLP-1R屬于G蛋白偶聯受體B簇中胰高血糖素受體亞家族,它的典型特征是具有一個七次跨膜的核心域和一個相對比較大的胞外域[2]。人的GLP-1R基因位于第6號染色體上,編碼463個氨基酸。胰腺內的GLP-1R主要表達在胰島β細胞中,除胰島外,GLP-1R還廣泛表達于胃、小腸、心臟、腎臟、肺及大腦等組織器官中[3]。顧名思義,GLP-1R的主要作用是和胰高血糖素樣肽-1(glucagon-like peptide-1 receptor, GLP-1)結合,調節血糖。
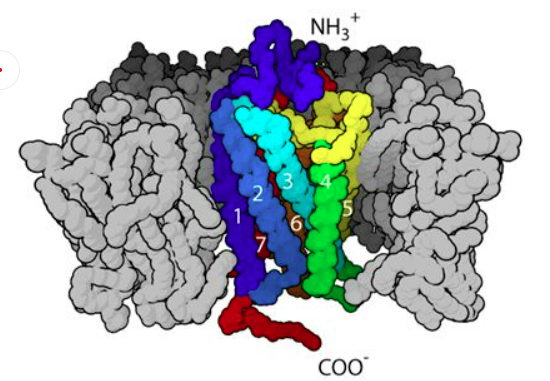
圖2 GLP-1R跨膜區三維結構
GLP-1
GLP-1是一種主要由腸道L細胞所產生的激素,屬于腸促胰素。GLP-1的半衰期非常短,僅1-2min,其發揮生理功能主要是通過結合并激活GLP-1R。人體內腸促胰素除GLP-1外還有葡萄糖依賴性胰島素釋放肽(GIP),但是只有GLP-1可以抑制胰高血糖素的釋放,引起飽足感[4]。截止到2021年,臨床上腸促胰素類藥物均基于GLP-1。
GLP-1R的功能
GLP-1R廣泛分布在胰島、胃、小腸、心臟、腎臟、肺、大腦等組織器官中,當它被GLP-1或人工合成的GLP-1R激動劑激活后,便能發揮多種不同的生理功能。在胰島細胞中,GLP-1R的主要作用是促進胰島β細胞的增殖,刺激胰島素的合成與釋放,并抑制胰高血糖素的合成與釋放。在胃腸道等組織中,GLP-1R可以抑制胃液分泌和胃腸道的蠕動,延遲胃的排空,增加飽食感,減少食物攝取[4]。在神經組織中,GLP-1R可以保護神經細胞,抵抗食欲不振,增強記憶力。在心血管方面,GLP-1R可以提升心血管的功能,減少炎癥[5]。
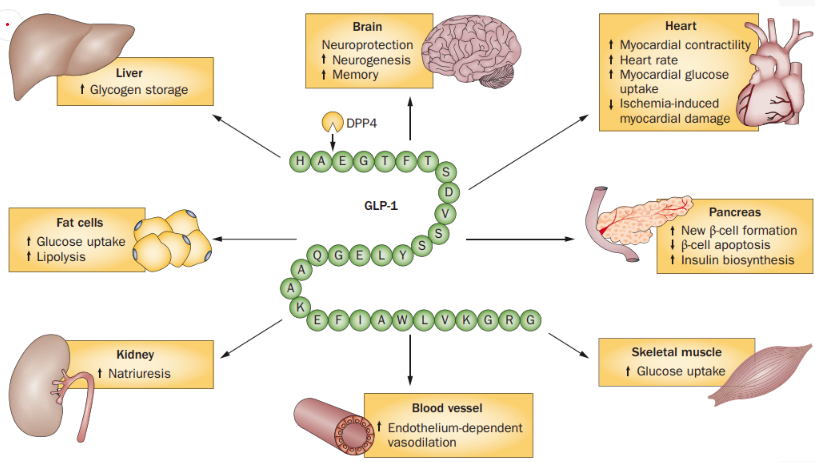
圖3 GLP-1R的生理功能
GLP-1R的激活
GLP-1R與配體的結合方式主要是大家熟知的“two-domain model”。配體的C端先同GLP-1R的胞外域結合,使GLP-1R的空間構象發生改變,暴露出核心域的結合位點,然后配體的N端同GLP-1R的核心域結合,激活GLP-1R。一般來說,GLP-1R胞外域的主要作用是識別特異性的配體,而核心域則在信號特異性傳導中發揮重要作用[6]。
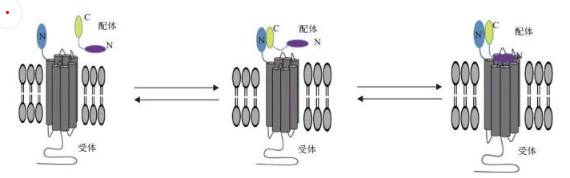
圖4 GLP-1R與配體結合的模式圖
GLP-1R信號轉導調控機制
GLP-1R是一種多效性偶聯受體,主要通過與多種G蛋白(Gαs、Gαi、Gαo和Gαq/11)偶聯來調控細胞通路。當與GLP-1結合后,GLP-1R在胰島β細胞中偶聯Gαs蛋白,激活腺苷環化酶,促使cAMP在細胞內含量升高,引起鈣離子內流,胰島素原基因轉錄增加,刺激血糖依賴性胰島素的分泌[7]。除此之外,GLP-1R還可以通過激活PI3K、MAPK和Ras/MAPK信號通路來促進胰島β細胞的增殖和分化。不僅如此,GLP-1R還能夠通過調控cAMP反應元件結合蛋白(CREB)和蛋白復活因子Bcl-2、Bcl-XL等來抑制細胞凋亡[8]。
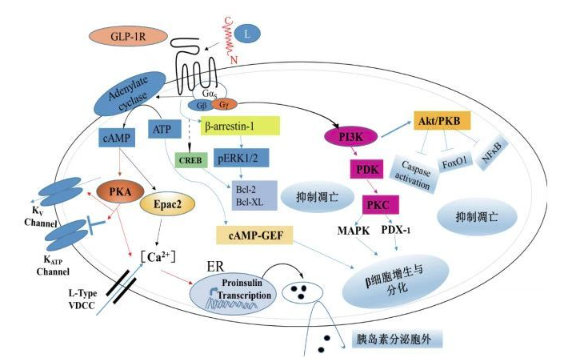
圖5 胰島β細胞中GLP-1R調控的信號通路
小分子非肽類GLP-1R激動劑
2019年諾和諾德宣布FDA批準其口服索馬魯肽(商品名Rybelsus)上市,成為全球首款口服GLP-1R激動劑。口服索馬魯肽的出現打破了糖尿病患者需要每天或每周注射藥物的現狀,備受市場關注,掀起了小分子非肽類GLP-1R激動劑藥物的研發狂潮!
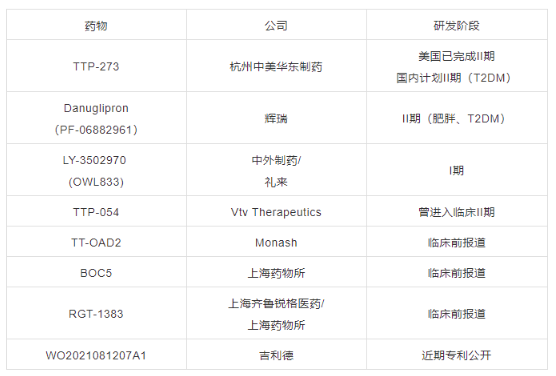
表1 在研小分子GLP-1R激動劑
GLP-1R人源化小鼠
鑒于GLP-1R在2型糖尿病藥物開發中的重要作用,上海南方模式生物科技股份有限公司(Shanghai Model Organisms Center,Inc.,簡稱“南模生物”)自主研發了GLP-1R人源化小鼠模型,為糖尿病藥物篩選,相關藥效實驗等研究提供了強有力的工具。
降血糖藥效驗證
GLP-1R人源化小鼠,在給藥和不給藥的條件下進行口服糖耐量(OGTT)實驗(n=5)。
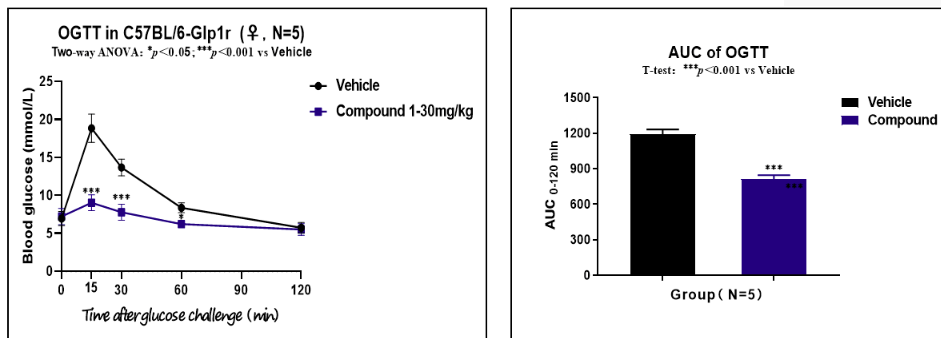
圖6 OGTT實驗(驗證數據由客戶提供)
結果顯示:針對人源GLP-1R,待測化合物表現出很好的降血糖效果(p<0.001)。上述數據證明,GLP-1R人源化小鼠模型,是進行糖尿病藥物篩選的有效工具。
南模生物深耕基因編輯領域,提供全方位模式生物服務,包括基因修飾成品模型供應、個性化模型定制、飼養繁育、表型分析、藥效評價等,滿足不同實驗室需求。
Reference:
[1]國際糖尿病聯盟 IDF 2019全球糖尿病地圖(第9版)
[2]Blad CC, Tang C, Offermanns S. G protein-coupled receptors for energy metabolites as new therapeutic targets. Nature Reviews Drug Discovery, 2012, 11 : 603–619.
[3]Pabreja K, Mohd MA, Koole C, et al. Molecular mechanisms underlying physiological and receptor pleiotropic effects mediated by GLP-1R activation. British Journal of Pharmacology, 2014, 171 : 1114–1128. DOI:10.1111/bph.12313
[4]Brubaker PL, Drucker DJ. Structure-function of the glucagon receptor family of G protein-coupled receptors: the glucagon, GIP, GLP-1, and GLP-2 receptors. Receptors & Channels, 2011, 8 : 179–188.
[5]Laviola L, Leonardini A, Melchiorre M, et al. Glucagon-like peptide-1 counteracts oxidative stress-dependent apoptosis of human cardiac progenitor cells by inhibiting the activation of the c-Jun N-terminal protein kinase signaling pathway. Endocrinology, 2012, 153 : 5770–5781. DOI:10.1210/en.2012-1461
[6]胡中平, 程念, 楊帆, 蘇正定. GLP-1R結構和功能及小分子藥物篩選研究進展[J]. 生物技術通報, 2017, 33(2): 30-40
[7]Dalle S, Ravier MA, Bertrand G. Emerging roles for β-arrestin-1 in the control of the pancreatic β-cell function and mass: New therapeutic strategies and consequences for drug screening. Cellular Signalling, 2011, 23 : 522–528. DOI:10.1016/j.cellsig.2010.09.014
[8]Robert G, Xiaomang Y, Baggio LL, et al. Cardiac function in mice lacking the glucagon-like peptide-1 receptor. Endocrinology, 2003, 144 : 2242–2252. DOI:10.1210/en.2003-0007




 17312606166
17312606166