在一項新的研究中,來自中國科學院深圳先進技術研究院的研究人員及其合作者開發出一種基因治療策略��,可選擇性地操縱受帕金森病影響的神經回路�,從而在嚙齒類動物和非人靈長類動物中減輕帕金森病的核心運動癥狀����。相關研究結果于2023年11月2日在線發表在Cell期刊上����,論文標題為“Circuit-specific gene therapy reverses core symptoms in a primate Parkinson’s disease model”。

帕金森病以中腦多巴胺能神經元(dopaminergic neuron)的喪失為特征,是老年人群中最常見的神經退行性疾病之一,影響著全球600多萬人。
表達多巴胺受體 D1的中型多棘神經元(medium spiny neuron�,下稱D1-MSN)和表達多巴胺受體D2的中型多棘神經元(下稱D2-MSN)占紋狀體中的90%神經元�。D1-MSN和D2-MSN都接受來自黑質致密部(substantia nigra pars compacta, SNc)的多巴胺能神經支配��,但在運動控制中卻扮演著截然相反的作用�。
投射到蒼白球內側部(globus pallidus internal segment, GPi)和黑質網狀部(substantia nigra pars reticulata, SNr)的 D1-MSN 構成直接通路并促進運動�。相反,投射到蒼白球外側部(globus pallidus external segment, GPe)的 D2-MSN則構成間接通路����,介導運動抑制����。
在帕金森病中����,多巴胺耗竭會導致這種直接通路的活動減退和這種間接通路的活動過度,從而引起多種運動癥狀�。
基于左旋多巴(Levodopa, L-Dopa)的治療有助于恢復這種多巴胺系統的功能����,是治療帕金森病的主要方法�。遺憾的是,幾乎所有長期接受左旋多巴治療的患者都會出現運動并發癥,比如運動波動和運動障礙��。因此����,精確、高效和穩定的治療方法非常必要����。
由于黑質網狀部接受來自D1-MSN的密集投射�,而沒有接受來自D2-MSN的投射����,這些作者提出,可以通過向黑質網狀部注射高效逆向腺相關病毒(adeno-associated virus, AAV)來選擇性標記D1-MSN�,然后通過在這種逆向AAV中引入神經元活動調節元件來專門操縱D1-MSN�。
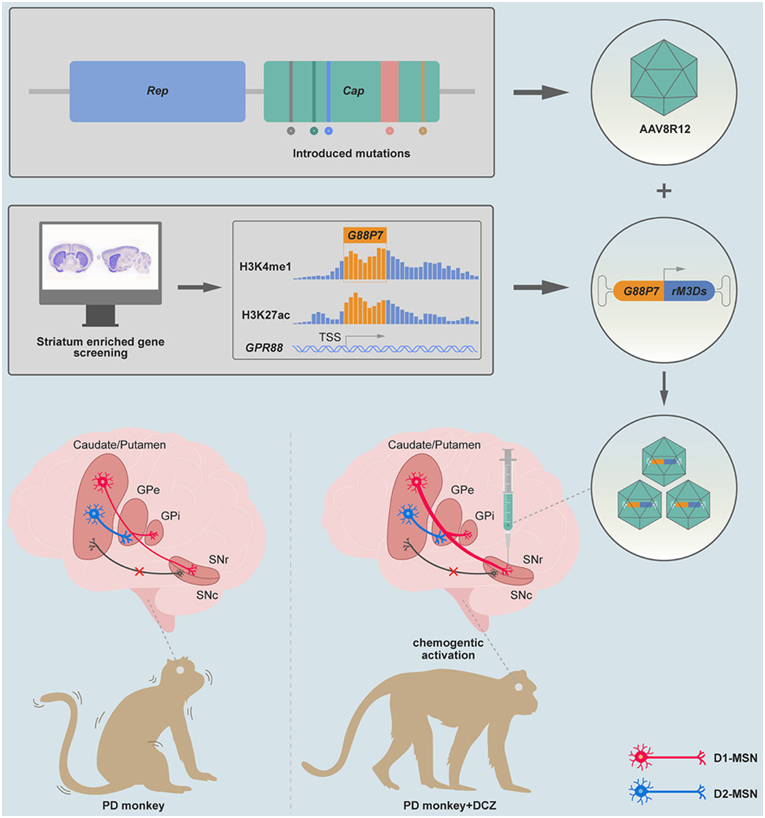
圖片來自Cell, 2023, doi:10.1016/j.cell.2023.10.004�。
為了實現上述目標,他們開發了一種新型 AAV衣殼AAV8R12����,用于對紋狀體中的 D1-MSN 進行高效逆向標記��,還開發了一種新的啟動子 G88P2/3/7,具有很強的 D1-MSN 活性�。這種基因治療策略利用化學效應物rM3D配合全身給送的激活藥物����,能夠特異性激活D1-MSN��,從而驅動D1-MSN介導的直接通路�。
在帕金森病靈長類動物模型中�,給送這種靶向 D1-MSN 的神經回路特異性基因療法后,運動遲緩、僵硬和震顫等典型運動癥狀得到了極大改善����。例如����,運動遲緩大大減少����,震顫完全消失,運動技能得到恢復�。
與左旋多巴治療非特異性地激活大腦和外周器官中的多巴胺系統不同�,這種新方法精確地操縱了D1-MSN介導的直接通路�。
與左旋多巴治療相比,這種操縱神經回路的基因療法不僅療效顯著��,而且起效更快�、持續時間更長����。單次給送后癥狀緩解持續時間超過 24 小時,而左旋多巴的典型治療窗口期為 6 小時��。在長期(即八個月以上)應用基因療法后��,左旋多巴治療后出現的運動障礙等運動并發癥消失了����。
除了顯示出治療帕金森病的潛力外�,這種操縱神經回路的基因療法還為未來開發治療其他腦部疾病的基于神經回路的靶向治療策略鋪平了道路。
參考資料:
Yefei Chen et al. Circuit-specific gene therapy reverses core symptoms in a primate Parkinson's disease model. Cell, 2023, doi:10.1016/j.cell.2023.10.004.
Circuit-specific gene therapy brings new hope for treatment of Parkinson's disease
https://medicalxpress.com/news/2023-11-circuit-specific-gene-therapy-treatment-parkinson.html




 17312606166
17312606166