早在1899年�����,Henschen教授便將運動員特有的大心臟稱為“運動員心臟(Athlete’s Heart)”���,認為“大心臟將在競賽中取勝”�����,因“運動員心臟”是對競技體育的良好的適應����。其主要表現在:運動性心動徐緩����、運動性心臟肥大和心臟泵血功能改善。其中,心臟肥大在力量運動員和耐力運動員中也不同�����,分別為室壁增厚和室腔變大[1]��。
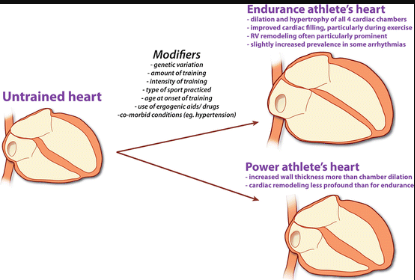
圖1 正常人和不同類型運動員心臟的區別[2]
也就是說運動員的心臟確實比正常人要大些。但是心肌肥大不是各類心血管疾病的前兆之一嗎����?難道不會對運動員的健康產生影響�����?
原來,心肌肥大可分為生理性的心肌肥大和病理性的心肌肥大。正常情況下,心臟肥厚生長是對血流動力學壓力的適應性反應�,它被認為具有增強心臟性能����、降低心室壁張力和耗氧量的代償作用。運動員的心肌肥大屬于生理性的。它是為了適應更大的運動量,主動做出的適應性改善�����,這種改變是溫和可逆的��,如果停止運動����,心臟的功能會恢復到正常水平[2,3]����。
另一種是病理性肥厚,常發生于高血壓和瓣膜病等慢性應激條件下,其特征是心室尺寸過度增大,伴有心肌功能障礙和纖維化。此外,肥厚心臟的心肌耗氧量增加�����,容易引起心肌供需不匹配�,進一步誘發多種心血管疾病��,包括心律失常��、心肌梗死、腦血管事件和猝死[3]�����。
那生理性心肌肥大和病理性心肌肥大有什么機制上的差異呢����?
首先,體液中存在的多種化學物質�����,例如激素����,生長因子,GPCR活化分子等��,廣泛參與心臟中大量的細胞過程����,在生理或者病理的刺激下,這些分子將激活不同的信號通路����,從而誘發不同類型的心肌肥大����。例如運動產生的刺激主要是通過IGF1-PI3K-Akt-mTOR信號通路�,促進心肌細胞生長和增殖。而高血壓等病理因素產生的刺激����,主要活化了MAPK-JNK通路,直接或間接增加了活性氧(ROS)的產生和代謝中間體在心肌細胞中的積累����,最終造成線粒體功能障礙�,細胞死亡和心肌纖維化[3,4]�����。
此外����,生理性和病理性心肌肥大的基因表達譜也有差異����。如胎兒基因ACTA1, MYH7, NPPA和NPPB在病理性心肌肥大患者中表達升高,但在生理性心肌肥大人群中的表達水平不變��,甚至下降[4]���。值得一提的是,炎癥也被證明是病理性心肌肥大的特征之一�,表現有巨噬細胞�、T淋巴細胞浸潤���,心肌纖維化����,相關炎癥因子的高表達等[3]。
看來生理性心肌肥大和病理性心肌肥大的分子基礎�,還是有很多不同的���。那如何預防或者抑制病理性心肌肥大呢?
南方醫科大學的廖禹林團隊通過一個有趣的實驗��,證實了運動產生的心肌肥大其實可以抵抗病理性的心肌肥大�。研究人員將小鼠分為2組��,其中實驗組小鼠也稱為回歸組�����,造模方法:對小鼠先進行21天游泳訓練,促使小鼠產生生理性心肌肥大,隨后終止運動��,讓小鼠的心肌恢復正常�����。對照組小鼠未經訓練��,稱為靜坐組。將回歸組與靜坐組小鼠同時進行主動脈縮窄(TAC)手術,構建病理性心肌肥大模型�。結果顯示��,在TAC手術后的第1和第4周,與靜坐組小鼠相比,回歸組小鼠的心肌肥厚增加較少�,Nppa和Myh7基因的表達較低�;在TAC手術后第4周��,回歸組小鼠的肺部充血減少�,左心室尺寸和舒張末期壓力較小����,綜上,回歸組小鼠的心肌對病理性刺激的抵抗力好于靜坐組[5]��。
看來運動確實可以預防病理性心肌肥大��,那如何抑制病理性心肌肥大呢?前面提及��,生理性心肌肥厚和病理性心肌肥厚的信號通路不同����。因此,通過抑制病理性心肌肥大的相關通路���,也可以達到抑制心肌肥大發展的效果。目前有比較多的靶向心肌細胞表面的激素受體的藥物����,如β-腎上腺素能受體拮抗劑����、血管緊張素轉換酶抑制劑和血管緊張素受體阻滯劑�����,可有效限制心臟肥大和心力衰竭的進展��,然而這種治療在某些患者中仍缺乏療效[6],因此新的機制和靶點分子亟待發現�。
前不久����,中國藥科大學齊煉文等人發現神經氨酸酶 1 (NEU1) 在小鼠和大鼠肥厚的心臟中高度表達��,并通過構建心臟條件性敲除Neu1小鼠�,驗證了這一基因對心肌肥厚的調控作用。實驗結果表明,NEU1 缺陷減輕了因主動脈收縮或腎上腺素輸注引起的心肌肥厚表型�。同時�����,研究人員也進行了NEU1 過表達�����,該蛋白的過表達加劇了心肌肥厚的發展����。此外����,抑制NEU1的藥物也起到了良好的心臟保護的效果[7]。這項工作將 NEU1 確定為心臟肥大的關鍵驅動因素��,并為心血管疾病的治療開辟了一個全新的領域����。這一文章也發表在European Heart Journal上(IF=29.98)。
實際上�,心肌肥大的發生發展是非常復雜的��,涉及多條信號通路和多種細胞?���;蛐揎椥∈竽P?��,可作為復雜信號研究的有力工具�����,并能夠指導靶向藥物的開發,在心肌肥大這一領域有著不可替代的優勢����。
[1] http://zjtks.tyj.zj.gov.cn/art/2019/9/25/art_1347729_38382581.html
[2] https://thoracickey.com/exercise-induced-right-heart-disease-in-athletes/
[3] Samak M, Fatullayev J, Sabashnikov A, et al. Cardiac Hypertrophy: An Introduction to Molecular and Cellular Basis. Med Sci Monit Basic Res. 2016 Jul 23;22:75-9.
[4] Nakamura M, Sadoshima J. Mechanisms of physiological and pathological cardiac hypertrophy. Nat Rev Cardiol. 2018 Jul;15(7):387-407.
[5] Lin H, Zhu Y, Zheng C, et al. Antihypertrophic Memory After Regression of Exercise-Induced Physiological Myocardial Hypertrophy Is Mediated by the Long Noncoding RNA Mhrt779. Circulation. 2021 Jun 8;143(23):2277-2292.
[6] Mehra MR, Uber PA, Francis GS. Heart failure therapy at a crossroad: Are there limits to the neurohormonal model? J Am Coll Cardiol. 2003;41(9):1606–10.
[7] Chen QQ, Ma G, Liu JF, et al. Neuraminidase 1 is a driver of experimental cardiac hypertrophy. Eur Heart J. 2021 Jun 28:ehab347.




 17312606166
17312606166