基因編輯小鼠是指通過基因編輯技術對特定目標基因進行“修飾”,從而在小鼠體內實現DNA片段的刪除或添加。基因編輯小鼠被廣泛用于研究基因對小鼠功能的影響,也被用于構建各種疾病模型,模擬人類疾病的發生發展過程以及相應藥物的研發。
基因編輯小鼠的制備方式主要有兩種,一種是ES細胞囊胚注射,另一種是受精卵顯微注射。無論哪種方式,基因編輯都是在受精卵水平進行操作,為了拿到基因編輯動物,則必須經過胚胎移植,在動物體內發育為完整的個體。
● 基于采用ES細胞囊胚注射方式獲得基因修飾小鼠的過程如下:
先對小鼠胚胎干細胞進行基因編輯,將基因打靶獲得的陽性ES細胞進行囊胚注射,再胚胎移植到假孕母鼠體內獲得高嵌合小鼠,高嵌合小鼠進一步與野生型小鼠進行交配,即可最終獲得基因編輯小鼠。
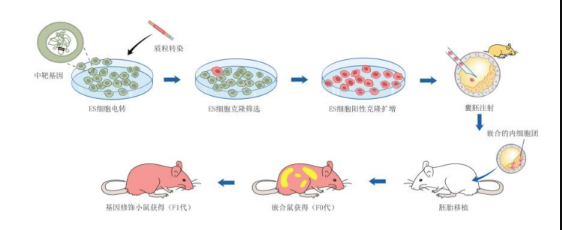
Fig.1 采用ES細胞囊胚注射方式獲得基因修飾小鼠的過程
● 基于受精卵顯微注射技術構建基因修飾小鼠的過程如下圖所示,
主要包括:gRNA設計和篩選,sgRNA表達載體構建,顯微注射,胚胎移植,小鼠繁殖等過程。
Fig.2 采用受精卵顯微注射方式獲得基因修飾小鼠的過程
胚胎移植除了可以用在基因編輯小鼠構建中,還有很多重要的應用:
凈化和快繁
為了保證小鼠的健康和疾病預防,一般外來小鼠必須經過隔離和凈化才能進入SPF級動物房。當前,凈化的主要技術是:體外受精(In Vitro Fertilization, IVF)+胚胎移植(Embryo Transfer, ET)技術(IVF-ET),其基本原理:小鼠自身雖然被感染,但小鼠的精子或卵細胞在體內是干凈無菌的。因此將雄鼠處死后取出精子,將精子激活后與超排的卵母細胞進行體外受精拿到受精卵,再移植到SPF級代孕小鼠的子宮中,這樣可以得到SPF級的小鼠后代。
IVF技術還具有一個重要應用--快速擴繁。使用IVF技術可短時間獲得大量子代小鼠,并且減少組內小鼠周齡差異,提高實驗數據一致性。應用于基因修飾小鼠則能夠一次性獲得大量相同基因型小鼠。
在小鼠進入動物房前,選擇IVF凈化服務,在凈化的同時,還能達到快速繁育的目的,同時獲得更多數目的子代鼠,效率高,縮短繁育周期,極大地加快科研進度。
挽救雄鼠不育的品系
單精子顯微注射技術(Intracytoplasmic sperm injection,ICSI),是指通過顯微操作系統將單個精子頭注入小鼠卵子胞漿內,再移植到代孕小鼠體內發育成小鼠的技術。該技術用于挽救因為精子無活力或者活力低造成雄性不育的小鼠品系。
胚胎(精子)復蘇
胚胎(精子)復蘇基于胚胎(精子)凍存技術,胚胎(精子)凍存常用于珍貴品系的保種,通過一定的降溫程序及保護措施將胚胎(精子)進行凍存,這種方法可以降低品系維持成本,且維持過程中不受疾病、不育等因素的影響。胚胎(精子)復蘇是指通過升溫的辦法將凍存的胚胎(精子)解凍,存活的胚胎體外培養一段時間后移植到代孕小鼠子宮內發育,進而獲得凍存品系小鼠活體的技術。其中胚胎凍存相比于精子凍存具有復蘇后存活率高、移植后懷孕率高的特點,具有明顯優勢,但其冷凍技術難度高,受限于專業機器--程序冷凍儀,建議交給專業機構來進行。
綜上所述,小鼠的胚胎移植技術是制備基因修飾動物、凈化、保種過程中的必需的、關鍵的技術手段,對于實驗動物學研究及生命科學研究具有重要價值。




 17312606166
17312606166