蒽環(huán)類藥物被廣泛用于各種實體瘤和血液系統(tǒng)惡性腫瘤的治療,包括多柔比星(Dox,又稱阿霉素)、伊達比星等。然而,盡管這類藥物在癌癥治療中具有良好的療效,但藥物會帶來心臟毒性,導致心律失常、心室功能障礙和心力衰竭等并發(fā)癥,從而嚴重影響患者的生活質量。因此,如何在不影響腫瘤治療效果的前提下設計適當?shù)寞煼▉韺苟嗳岜刃钦T導的心臟毒性,成了擺在研究人員面前的一道難題。
一些研究表明,熱量限制(CR)不僅能有效抗癌,還能顯著改善化療引起的毒性。不過,這種方法在臨床上的應用仍然有限,因為大多數(shù)患者很難堅持長期節(jié)食。目前的證據(jù)表明,組蛋白去乙酰化酶SIRT6可以模擬熱量限制對壽命延長的影響,并改善葡萄糖穩(wěn)態(tài)。SIRT6是許多癌癥中的抑癌基因,可以催化組蛋白H3K9、H3K18和H3K56去乙酰化,在細胞代謝、DNA損傷修復、炎癥反應等多個生理進程中發(fā)揮重要作用。
近日,清華大學藥學院王釗教授領導的研究團隊發(fā)現(xiàn),去乙酰化酶SIRT6可作為一種有效的治療靶點,在減輕蒽環(huán)類藥物心臟毒性的同時增強其抗腫瘤活性。這項研究成果發(fā)表在《Acta Pharmaceutica Sinica B》雜志上,突出了SIRT6在線粒體穩(wěn)態(tài)中的關鍵作用,為緩解蒽環(huán)類藥物的心臟毒性提供了一種可行且有前景的臨床干預策略。

圖片來源:《Acta Pharmaceutica Sinica B》
(https://doi.org/10.1016/j.apsb.2023.03.019)
研究材料與方法
研究人員在本研究中使用了SIRT6過表達小鼠(由賽業(yè)生物提供),并在此小鼠的基礎上通過注射多柔比星建立了慢性和急性的小鼠心臟毒性模型。此外,作者還通過移植小鼠肺癌細胞(LLC)構建了小鼠荷瘤模型。體外研究主要在小鼠心肌細胞、Lewis肺癌細胞、乳腺癌細胞等細胞系上開展。在分析線粒體穩(wěn)態(tài)時,研究人員測定了細胞的耗氧率(OCR)、胞外酸化率(ECAR)和ATP生成速率。
技術路線
01通過分析乳腺癌患者的血液樣本,發(fā)現(xiàn)SIRT6表達在蒽環(huán)類藥物化療后下降
02在體外和體內實驗中評估SIRT6過表達是否可改善Dox誘導的心臟毒性
03在荷瘤小鼠模型上評估SIRT6過表達是否可增強Dox的抗腫瘤效果
04從機制上分析SIRT6過表達如何對心肌細胞和腫瘤細胞產(chǎn)生不同影響
05評估鞣花酸(SIRT6激動劑)是否可減輕Dox誘導的心臟毒性
研究結果
1.癌癥患者化療后SIRT6表達下降
在此次研究中,研究人員選取了10位乳腺癌患者,在化療前采集血液樣本,并在4個周期的蒽環(huán)類藥物治療后再次采集樣本,用于檢測患者血漿中SIRT6的表達水平和乳酸濃度變化。在經(jīng)過4個周期的化療后,患者血漿中的SIRT6水平較治療前明顯下降,這表明化療抑制了SIRT6的表達。同時,治療后患者血漿中的乳酸濃度明顯高于治療前,證實了糖酵解的增加與化療有關。這些結果表明,SIRT6的減少和糖酵解的增加與蒽環(huán)類藥物誘導的毒性有關。
2.SIRT6過表達可改善Dox誘導的心臟毒性
那么,SIRT6過表達是否能改善Dox誘導的心臟毒性?研究人員從由賽業(yè)生物提供的SIRT6過表達小鼠(TG)和野生型小鼠(WT)中分離出原代心肌細胞,并用不同濃度的Dox處理細胞。在接受處理后,TG心肌細胞的存活率明顯高于WT心肌細胞。之后,作者通過慢病毒載體構建了多個過表達SIRT6的細胞系,發(fā)現(xiàn)SIRT6過表達可以降低Dox對心肌細胞的毒性,同時增強Dox對腫瘤細胞的毒性。
為探究SIRT6過表達能否在體內改善Dox誘導的心臟毒性,研究人員以SIRT6過表達小鼠為研究對象,建立了慢性(5周低劑量治療)和急性(2周高劑量治療)的Dox誘導心臟毒性小鼠模型(圖1)。
在慢性心臟毒性模型中,野生型小鼠在接受Dox治療后出現(xiàn)了心臟功能障礙,而過表達小鼠的心臟功能障礙并不明顯,表明SIRT6的過表達可改善Dox誘導的心臟功能障礙(圖1)。此外,SIRT6過表達可顯著緩解Dox誘導的心力衰竭癥狀,并減少Dox誘導的心肌細胞凋亡和心臟纖維化。在急性心臟毒性模型中,SIRT6過表達可以顯著延長Dox治療小鼠的生存期。這些結果與體外數(shù)據(jù)一致,表明SIRT6可能是治療Dox誘導的心臟毒性的有效靶點。

圖1 SIRT6過表達改善了Dox誘導的小鼠心臟毒性[1]
3.SIRT6過表達可增強Dox的抗腫瘤效果
為了確定SIRT6過表達是否能增強Dox在小鼠體內的抗腫瘤效果,研究人員通過注射LLC細胞制備出荷瘤小鼠,并用Dox或生理鹽水處理兩周。與生理鹽水相比,Dox處理可抑制腫瘤生長。值得注意的是,SIRT6過表達可顯著增強Dox介導的腫瘤消退。Ki67免疫熒光染色和TUNEL染色的結果顯示SIRT6過表達可以顯著增強Dox介導的抗增殖和促凋亡活性,表明SIRT6過表達可顯著增強Dox的抗腫瘤效果。這些結果證實,SIRT6過表達可以作為Dox治療過程中的一種輔助策略。
4.SIRT6過表達可增強線粒體呼吸并抑制糖酵解
之后,研究人員深入探索了Dox誘導心臟毒性的分子機制。對原代心肌細胞的RNA測序結果顯示Dox處理后差異表達的基因高度集中于代謝通路,表明Dox誘導的代謝變化可能是造成心臟毒性的原因。通過線粒體呼吸和糖酵解分析,作者發(fā)現(xiàn)心肌細胞和腫瘤細胞的線粒體呼吸均因Dox處理而顯著降低,同時糖酵解均顯著增加,這表明細胞的代謝模式從線粒體呼吸向糖酵解轉變。此外,透射電鏡觀察結果表明Dox破壞了線粒體結構以及線粒體DNA的完整性。
那么,SIRT6過表達是否可逆轉Dox誘導的糖酵解轉變?研究人員發(fā)現(xiàn),在過表達SIRT6的心肌細胞和腫瘤細胞中,Dox誘導的呼吸能力降低被顯著逆轉,而糖酵解也被抑制,表明SIRT6過表達介導了從糖酵解到線粒體呼吸的轉變。那么問題來了,既然SIRT6對心肌細胞和腫瘤細胞的代謝調控作用相同,為什么兩種細胞在過表達SIRT6后對Dox的敏感性出現(xiàn)差異?
事實上,腫瘤細胞和心肌細胞的代謝模式不同。大多數(shù)腫瘤細胞依賴糖酵解產(chǎn)生ATP,這被稱為Warburg效應;心肌細胞則以線粒體呼吸作為主要的能量來源。研究人員通過一系列實驗證實,在Dox處理過程中,SIRT6介導的從糖酵解到線粒體呼吸的代謝重塑更適合心肌細胞的存活,而不是腫瘤細胞的存活(圖2)。

圖2 SIRT6過表達差異調節(jié)了心肌細胞和腫瘤細胞的ATP生成[1]
通過RNA測序分析,作者發(fā)現(xiàn)SIRT6抑制了Sgk1的轉錄,此基因編碼了血清和糖皮質激素調節(jié)激酶1。后續(xù)分析發(fā)現(xiàn),SIRT6通過調控Sgk1啟動子區(qū)域的組蛋白乙酰化而直接抑制了Sgk1的表達,從而影響了線粒體的生物合成和線粒體自噬。
5.鞣花酸可減輕Dox誘導的心臟毒性
之前的研究證實,鞣花酸作為一種SIRT6激動劑,可增加腫瘤細胞中的SIRT6表達。因此,研究人員分析了鞣花酸是否能緩解Dox誘導的心臟功能障礙,同時增強Dox的抗腫瘤效果。實驗結果顯示,鞣花酸處理增加了SIRT6的表達,激活了SIRT6的去乙酰化作用,同時降低了Dox誘導的心肌細胞凋亡,增強了Dox誘導的腫瘤細胞凋亡。在小鼠體內實驗中,鞣花酸在減輕Dox誘導的心臟毒性的同時,增強了Dox介導的腫瘤消退。
研究結論
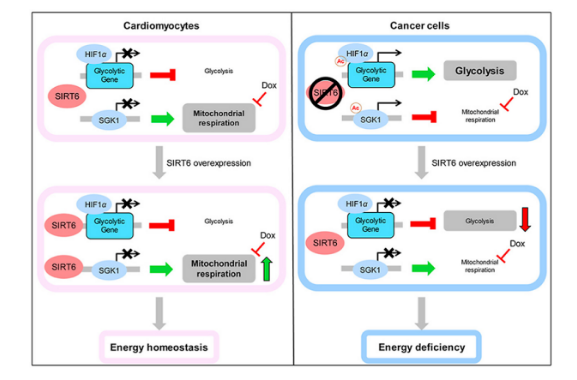
圖3 SIRT6過表達對心肌細胞和腫瘤細胞的不同影響[1]
總的來說,這項研究強調了SIRT6在線粒體穩(wěn)態(tài)中的關鍵作用。SIRT6作為組蛋白H3K9的去乙酰化酶抑制糖酵解,增強線粒體呼吸,從而導致代謝重塑,這與心肌細胞的代謝模式相適應(圖3)。考慮到SIRT6的激活可以緩解Dox誘導的心臟毒性,同時增強Dox的抗腫瘤效果,作者建議將SIRT6的靶向激活作為預防或治療蒽環(huán)類藥物引發(fā)的心臟毒性的一種可行策略。同時,這項研究也為鞣花酸作為化療患者的輔助療法提供了臨床前依據(jù)。
原文檢索:
[1]Peng, K., Zeng, C., Gao, Y., et al. Overexpressed SIRT6 ameliorates doxorubicin-induced cardiotoxicity and potentiates the therapeutic efficacy through metabolic remodeling. Acta Pharm. Sin. B. 2023 Jun;13(6): 2680-2700. https://doi.org/10.1016/j.apsb.2023.03.019




 17312606166
17312606166