近日,中國科學(xué)院合肥物質(zhì)院健康與醫(yī)學(xué)技術(shù)研究所韓偉團(tuán)隊(duì)發(fā)現(xiàn),膳食中的花生四烯酸會(huì)促進(jìn)放射性腸損傷發(fā)生。相關(guān)研究成果發(fā)表在Redox Biology上。
放射性腸損傷(Radiation-induced intestinal injury)是腹盆腔及腹膜后腫瘤放療時(shí)常見的腸道并發(fā)癥(發(fā)病率約80%),嚴(yán)重時(shí)或?qū)е路暖熤袛嗖⑽:】担壳芭R床尚無放射性腸損傷的治療方法。因此,確定放射性腸損傷的發(fā)病機(jī)制,是發(fā)展放射性腸損傷治療策略的重要前提。
該團(tuán)隊(duì)對存在放射性腸損傷癥狀的小鼠的腸組織進(jìn)行轉(zhuǎn)錄組測序,發(fā)現(xiàn)該現(xiàn)象可能與小鼠體內(nèi)鐵死亡相關(guān)。研究顯示:存在放射性腸損傷癥狀的小鼠腸組織中檢測到鐵死亡標(biāo)志物——4-羥基壬烯醛和丙二醛的水平顯著上升;而鐵死亡抑制劑Ferrostatin-1能有效緩解放射性腸損傷小鼠的死亡和腸道纖維化。在細(xì)胞、小腸類器官和小鼠模型中,研究均發(fā)現(xiàn)Omega-6型必需脂肪酸——花生四烯酸(Arachidonic acid,AA)是放射引發(fā)鐵死亡的關(guān)鍵因素。外源性花生四烯酸能誘發(fā)放射導(dǎo)致細(xì)胞鐵死亡。機(jī)制研究發(fā)現(xiàn):放射后STAT1-IRF1活化正向調(diào)控ACSL4表達(dá),會(huì)促進(jìn)放射后鐵死亡的發(fā)生;而AMPK信號(hào)通路受AA激活,對放射誘導(dǎo)的鐵死亡起一定負(fù)調(diào)控作用。
研究表明,STAT1-IRF1-ACSL4和AMPK信號(hào)通路有望成為放射性腸損傷防治策略研發(fā)的潛在分子靶點(diǎn)。人體膳食中的必需脂肪酸——花生四烯酸是鐵死亡介導(dǎo)放射性腸損傷發(fā)生的重要風(fēng)險(xiǎn)因素。該研究提出了在放療中應(yīng)當(dāng)有針對性的進(jìn)行膳食營養(yǎng)管控,有望緩解放射性腸損傷。
研究工作得到國家自然科學(xué)基金、合肥物質(zhì)院院長基金、合肥市綜合性國家科學(xué)中心入庫項(xiàng)目和安徽省重點(diǎn)研發(fā)計(jì)劃等的支持。
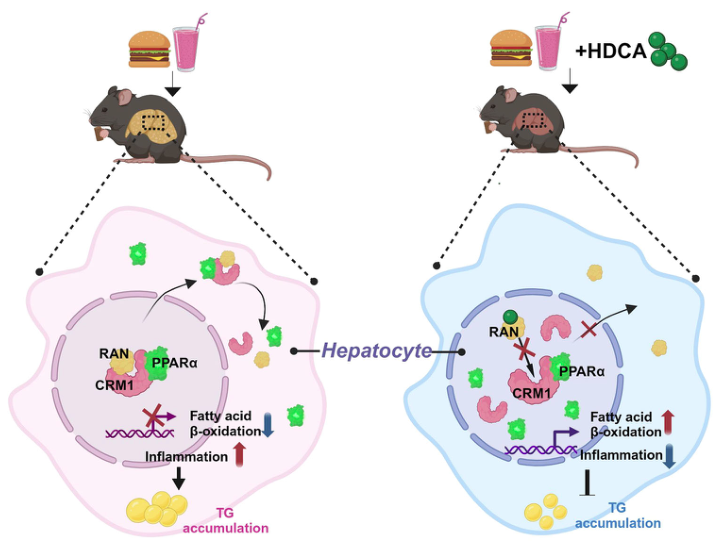
鐵死亡介導(dǎo)放射腸損傷機(jī)理




 17312606166
17312606166 加微信獲取對接
加微信獲取對接